這一周是令國人無比悲憤的一周,因為假疫苗事件帶來了極為惡劣的影響。那么如何能通過技術手段,有效防止生產(chǎn)數(shù)據(jù)造假呢?
這些年我們經(jīng)歷了奶粉、雞蛋、D溝油等一波波的侵擾,這幾天我們又被一起醫(yī)藥制造的事件刷屏了,靜下來,想一想,應該少一些抱怨和憤慨,努力去做點什么,想想醫(yī)生該做些什么?醫(yī)院該做些什么?經(jīng)銷商該做些什么?公務員該做些什么?工程師該做些什么?父母們該做些什么?企業(yè)家該做些什么?企業(yè)管理者該做些什么?企業(yè)員工該做些什么?
如何能夠避免類似事件再次發(fā)生,是我們該想的,每一個崗位的人員都恪盡職守,認真負責,是我們力所能及該做的,不能等出了事,大家不辨真假一擁而上。因為,當下一個災難來臨的時候,或許大家都已不是局外人。
企業(yè)編造生產(chǎn)記錄和產(chǎn)品檢驗記錄,并隨意變更工藝參數(shù)和設備,這即是人工有意為之,性質也是非常不好的,在國外應該算是刑事案件吧,CFDA的檢查起到了非常關鍵的作用,其實在這方面,MES數(shù)字化制造管理平臺可以很好的解決數(shù)據(jù)造假的問題,通過數(shù)字化制造平臺建設,促進企業(yè)生產(chǎn)制造過程對工藝參數(shù)、設備及人員資質、原材料及零部件等進行強制性和透明化管控或下發(fā),通過工藝建模數(shù)據(jù)審計跟蹤、制造數(shù)據(jù)審計跟蹤、設備數(shù)據(jù)審計跟蹤等多維度、多視角幫助企業(yè)、FDA、CFDA把好工藝關、生產(chǎn)關、物料關、質量關、數(shù)據(jù)關,讓制造企業(yè)的"數(shù)字化五官“更端正,更可靠,更經(jīng)得起審查和推敲。
與其他行業(yè)相比,制藥以醫(yī)療器械制造企業(yè)具有工藝機理復雜、不確定因素多、企業(yè)生產(chǎn)計劃性強、生產(chǎn)調度管理繁瑣、批號管理嚴格等特殊性。主要體現(xiàn)在:
① 合規(guī)性要求高:
從藥品研發(fā)、中試、臨床至注冊申請通過,訂單下達到生產(chǎn)完成全部生產(chǎn)活動都要符合FDA、CFDA、GxP等法規(guī)要求下進行;藥品生產(chǎn)每批都有完整的數(shù)據(jù)記錄要求,從原輔料,中間品到最終銷售的成品,包括批號、數(shù)量、重量、時間、人員、設備環(huán)境參數(shù)、偏差等,都要被準確、實時、可靠的記錄。
② 工藝復雜及產(chǎn)能受限:
生產(chǎn)過程包含復雜的物理和生化過程,上下游物料之間的數(shù)量關系可能隨溫度、濕度、季節(jié)、人員技術水平、工藝條件的不同而不同。對生產(chǎn)工藝和先進控制,如設備嚴密性、生產(chǎn)操作、環(huán)境的要求極其嚴格。制藥企業(yè)主要是大批生產(chǎn),只有滿負荷運行,才能將成本降低,通過配方和訂單或需求預測制定物料需求計劃,但受生產(chǎn)能力限制。
③ 完善的質量管理體系:
質量管理體系是組織內部建立的、為實現(xiàn)質量目標所必需的、系統(tǒng)的質量管理模式,是組織的一項戰(zhàn)略決策;企業(yè)必須建立完善的質量管理體系以確保生產(chǎn)運作活動都是在符合規(guī)范的條件下進行的,所有程序都應書面化和標準化。
合規(guī)與品質是他們賴以生存的基礎,而數(shù)據(jù)完整性又是企業(yè)持續(xù)合規(guī)與質量度量的基石。數(shù)據(jù)完整性不僅是質量控制問題,也是貫串研發(fā)、注冊、生產(chǎn)、質量、到變更等整個產(chǎn)品周期,是人、機、料、法、環(huán)、測的全過程數(shù)據(jù)收集與管控。按照美國法律,GMP合規(guī)問題是民事問題,而數(shù)據(jù)完整性問題是刑事問題。由此也可以看出,篡改數(shù)據(jù)在國外是一件非常嚴重的問題,也是在FDA審核時會被追問或者整改的重點,嚴重的可能不會通過FDA的審核。
在數(shù)字化制造過程中,制造執(zhí)行系統(tǒng)MES具備將生產(chǎn)產(chǎn)線與企業(yè)資源計劃系統(tǒng)以及底層設備承上啟下的聯(lián)接作用,企業(yè)通過MES與ERP,生產(chǎn)設備的連接,即時掌握生產(chǎn)現(xiàn)場狀況,迅速做出決策。
數(shù)字化制造MES系統(tǒng)概括來講
可以為企業(yè)管理帶來如下優(yōu)勢
無紙化制造,降低人為錯誤提高制造數(shù)據(jù)的數(shù)字化和結構化比率
MES將企業(yè)資源計劃系統(tǒng)的生產(chǎn)計劃具體分配到各個生產(chǎn)工序,使用主動式制造執(zhí)行替代人工紙質制造流程,可以簡化流程、降低成本以及提高質量和合規(guī)性。其結果是,可以為所有制造活動提供完整的電子審查追蹤并支持電子設備歷史記錄eDHR。無需用紙質記錄、打印、轉移或存儲。
自動化執(zhí)行和控制讓設備制程參數(shù)從MES下發(fā)和記載并在設備上自動執(zhí)行
通過收集信息和執(zhí)行業(yè)務規(guī)則,有效防止流程出錯。通過數(shù)據(jù)接口,自動采集環(huán)境參數(shù)、設備狀態(tài)參數(shù)和運行參數(shù)等以保障生產(chǎn)全流程數(shù)據(jù)完整性,實現(xiàn)高效率的生產(chǎn)運行,生產(chǎn)全流程可視化、標準化。確保所用的生產(chǎn)流程、操作員、設備和物料合理、有序。根據(jù)自動“內部審查”電子設備歷史記錄,移至“按異常審核”產(chǎn)品放行流程。減少人為干預或數(shù)據(jù)記錄的工作,針對錯誤操作,系統(tǒng)支持修改,但錯誤操作記錄將被永久保存到系統(tǒng)中。讓MES執(zhí)行的每一項事務都可以得到追溯和還原。
精益生產(chǎn)和六西格瑪,降本增效確保人、機、料、法、環(huán)的正確應用
可嚴格控制經(jīng)過訓練(以操作員培訓和認證模組為支撐)的工作人員按照SOP(標準操作程序)執(zhí)行每一步操作,通過管理負責人的操作確認和批準、電子簽名等措施,加強生產(chǎn)現(xiàn)場管理和質量控制。精益生產(chǎn)與六西格瑪方案可通過數(shù)據(jù)來確立基準、發(fā)現(xiàn)需要改進的方面、分析結果并控制流程。MES可讓您在數(shù)秒之內按照結構化電子格式收集綜合性產(chǎn)品、流程和質量數(shù)據(jù)。通過系統(tǒng)化的執(zhí)行來確保控制,以防止流程出錯,并通過閉環(huán)反饋實現(xiàn)持續(xù)改進。
全局流程數(shù)據(jù)管理讓工藝、變更、檢驗數(shù)據(jù)有源可循
為任一全球工廠定義、分發(fā)和執(zhí)行流程及工程變更。通過全面審查追蹤,可以了解工程更改命令 (ECO) 的影響以及糾正和預防措施的效果。根本原因智能分析可利用不斷增長的知識庫發(fā)現(xiàn)問題的真正來源,該知識庫中包括詳細產(chǎn)品設計、流程設計、制造(完工和檢驗)、現(xiàn)場使用和質量事件數(shù)據(jù)。
審核控制管理和正向、逆向追溯自動審查eDHR
利用可配置調查( 例如用途反查分析)根據(jù)標準(例如組件批次、機器、操作員、特定班次等)發(fā)現(xiàn)存在風險的可疑物料。根據(jù)您的業(yè)務規(guī)則配置動態(tài)操作,然后快速采取措施,例如扣留、返工、提交物料評審委員會 (MRB) 和隔離等。所有產(chǎn)品、組件和已供應物料均全程可追溯。
統(tǒng)計過程控制SPC建立動態(tài)質量控制體系
對于在制造流程期間采集的質量和檢測數(shù)據(jù)實施統(tǒng)計過程控制,使制造商可以發(fā)現(xiàn)、分析、解決和預防可能存在的問題, 并保證生產(chǎn)過程不受影響。減少物料生產(chǎn)延誤、設備停機時間和報廢。
 2025-07-14
培訓賦能AI化工升級,客戶價值驅動產(chǎn)業(yè)創(chuàng)新
2025-07-14
培訓賦能AI化工升級,客戶價值驅動產(chǎn)業(yè)創(chuàng)新
夏日的煙臺,海風送爽。在第十屆煙臺國工智能科技有限公司AI研究院“AI課題文獻綜述分享茶歇會”上,一場聚焦“人工智能與化工領域深度融合”的智慧盛宴成功舉辦。
6月9日,第八屆煙臺國工智能科技有限公司AI研究院“AI課題文獻綜述分享茶歇會”成功舉辦。本次會議聚焦“基于遺傳算法的高分子配方設計方法”,通過前沿技術分享與案例解析,展現(xiàn)了國工智能在AI+材
 2024-11-13
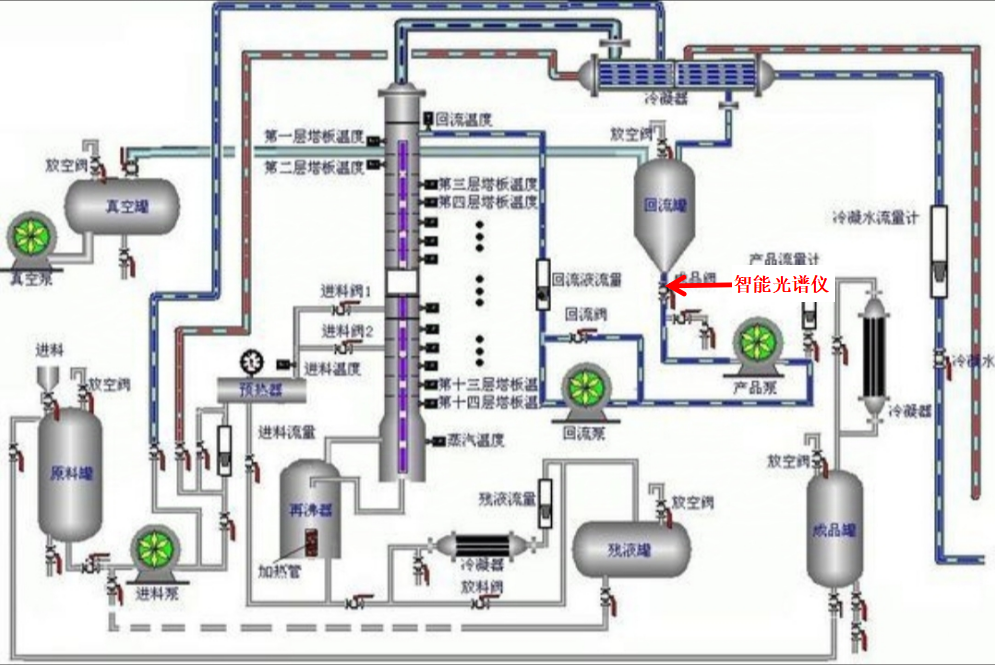
智能光譜儀在四氫呋喃精餾回收工藝在線檢測的應用
2024-11-13
智能光譜儀在四氫呋喃精餾回收工藝在線檢測的應用
精餾回收工藝是醫(yī)藥化工行業(yè)中的最為重要的典型單元操作之一,在原料藥、精細化工、輕工業(yè)等各個領域都有極其廣泛的應用。由于精餾過程的復雜性,精餾工藝過程的終點現(xiàn)階段仍需要生產(chǎn)工人每隔一定時間取樣送實驗室檢測,通過氣相色譜測定含量,卡爾費休滴定法
 2023-09-28
月圓人圓,國工與您賀中秋迎國慶!
2023-09-28
月圓人圓,國工與您賀中秋迎國慶!
中秋節(jié)是中國傳統(tǒng)節(jié)日之一,也是一年中最重要、最盛大的節(jié)日之一。在這一天,以明亮的月亮和家人團聚為特點,承載著人們無盡的思念和美好的祝福。 國慶、中秋兩節(jié)遇, 合家團圓精神俱。 團團圓圓過中秋, 歡歡喜喜